-* Auteurs : Dr Stéphane VIGNES, Pr Dominique FARGE
Service de médecine inteme, Hôpital Saint-Louis, Paris
Nous sommes conscients que cet article est relativement ancien; toutefois, il renferme des renseignements qui vous seront sans doute utiles; aussi l’avons-nous laissé en ligne. Par ailleurs, si vous disposiez d’articles plus récents sur le même sujet, n’hésitez pas à nous en faire part afin de demander leur autorisation à leurs auteurs pour une publication en ligne sur ce site
Points Forts à Comprendre
Les antigènes d’histocompatibilité du donneur sont les principales cibles du rejet de greffe d’organes.
La réaction du greffon contre l’hôte est le mécanisme inverse du rejet d’allogreffe : les antigènes du receveur deviennent la cible des cellules du donneur.
L’IL-2, produite par les Iymphocytes CD4+, est la principale cytokine au cours de la réaction de rejet.
Revenir au menu
Les mécanismes immunologiques complexes du rejet d’une allogreffe et de la maladie du greffon contre l’hôte font intervenir les différents éléments du système immunitaire qui concourent au rejet du non-soi par deux processus complémentaires : l’immunité cellulaire, dépendant principalement des cellules T et des cytokines, et l’immunité humorale, médiée par les anticorps produits par les cellules B. Le système immunitaire, dont le rôle est de protéger l’individu contre toute substance étrangère, est caractérisé par sa spécificité pour l’antigène, sa capacité à distinguer les antigènes du soi et du non-soi et enfin par sa mémoire pour permettre une réponse anamnestique plus forte lors de la réintroduction de l’antigène initial. Parmi les nombreuses substances antigéniques faisant l’objet d’un polymorphisme au sein de l’espèce (allotypes), la principale cible du rejet de greffe est l’ensemble des antigènes tissulaires, codés par des gènes exprimés à la surface des membranes cellulaires, définissant les systèmes d’histocompatibilité. Trois principaux systèmes interviennent dans le rejet de greffe:
1) le système des groupes sanguins ABO et Lewis correspond à des molécules tissulaires très fortement antigéniques;
2) le système HLA (Human Leucocyte Antigen) code pour l’identité du soi (HLA classe 1) et le contrôle du rejet du non-soi (HLA classe II);
3) un ensemble d’autres systèmes d’histocompatibilité appelés mineurs qui codent pour des antigènes de transplantation présentés sous forme de peptides en association avec les produits du complexe majeur d’histocompatibilité (CMH) du donneur ou du receveur.
L’expression clinique du rejet d’allogreffe est étroitement liée à la nature de l’organe greffé, à l’intensité du rejet (suraigu, aigu ou chronique) et aux possibilités de manipuler la réponse immunologique du receveur afin d’éviter la réaction de rejet par le receveur en cas de greffe d’organe, ou par le greffon lui-même vis-à-vis de son hôte en cas de greffe de moelle.
Revenir au menu
Définitions
Autogreffe: greffe d’organe ou de tissus lorsque donneur et receveur sont le même individu.
Greffe syngénique: greffe d’organe ou de tissus d’un donneur à un receveur génétiquement identique (jumeaux homozygotes).
Allogreffe: greffe d’organe ou de tissus d’un donneur à un receveur génétiquement différent au sein d’une même espèce.
Xénogreffe ou hétérogreffe: greffe d’organe ou de tissus d’un donneur à un receveur appartenant à deux espéces animales différentes.
Revenir au menu
Principaux éléments du système immunitaire impliqués dans le rejet de greffe et de la maladie du greffon contre l’hôte
Cellules
1. Cellules présentant l’antigène
Les cellules de la lignée monocytes-macrophages, comprenant les monocytes du sang circulant et les macrophages tissulaires, constituent les principales cellules présentatrices d’antigènes aux lymphocytes T. L’antigène étranger est capté, internalisé, puis dégradé par une action enzymatique. Cette transformation produit des peptides allogéniques, qui sont ensuite exprimés à la surface des monocytes macrophages en association avec les molécules HLA de classe II. Cette étape s’accompagne, entre autres, de la sécrétion de cytokines (Tumor necrosis factor a, interleukine 1, interleukine 6) et d’enzymes (protéases, Iysozyme) par le monocyte-macrophage. D’autres cellules non phagocytaires peuvent intervenir dans la présentation de peptides allogéniques, notamment les cellules dendritiques du thymus et des tissus, les cellules de Langerhans de l’épiderme et des Iymphocytes B.
2. Lymphocytes T
Ils ont un rôle majeur dans la réponse immunitaire cellulaire et agissent directement comme cellules effectrices. Chez l’homme, tous les Iymphocytes T expriment le récepteur CD2, mais la voie majeure d’activation Iymphocytaire T dépend de l’acquisition d’un récepteur TCR (T Cell Receptor) spécifique de l’antigène et couplé au CD3 sous la forme d’un complexe CD3/TCR à la surface cellulaire, qui rend les cellules T immunologiquement fonctionnelles. Le complexe CD3 transmet à 1’intérieur de la cellule un signal d’activation lorsque le TCR est stimulé par l’antigène.
Trente pour cent des Iymphocytes T circulants expriment le récepteur CD8, qui reconnaît les antigènes d’histocompatibilité de classe I. Deux types de lymphocytes T portent le marqueur CD8: les lymphocytes T cytotoxiques exerçant une cytotoxicité directe sur les cellules cibles sans l’intermédiaire d’une cellule présentatrice d’antigènes et les Iymphocytes T suppresseurs qui modulent l’activité des cellules B et T.
Soixante-dix pour cent des Iymphacyles T circulants expriment le marqueur CD4. Ils sont appelés Iymphocytes T auxiliaires ou « helper » et reconnaissent les antigènes d’histocompatibilité de classe II. Ils participent à la transformation des Iymphocytes B en cellules productrices d’anticorps et à la différenciation des cellules T cytotoxiques. On distingue 2 types de sous-populations Iymphocytaires CD4+ selon leur profil de sécrétion de cytokines après stimulation antigénique: 1) les CD4+ Thl sécrètent de l’interleukine 2 (IL-2), de 1’interféron gamma (IFN gamma), activent les macrophages et sont également responsables de l’hypersensibilité retardée; 2) les Iymphocytes CD4+ Th2 secrètent de l’IL-4, de 1’IL-5 et de 1’IL-10, entrament la production d’IgE, la stimulation des éosinophiles et des mastocytes. Les Iymphocytes T CD4+ Thl exercent une action inhibitrice sur les Th2 et réciproquement.
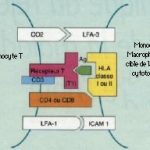
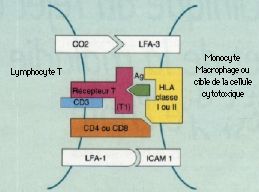
Molécules d’adhésion : les interactions cellulaires font intervenir avec l’adhésion des Iymphocytes T, différents types de cellules: les macrophages, les cellules B avec lesquelles ils coopèrent, et les cellules-cibles d’une réaction de cytotoxicité. Le CD31TCR établit une liaison spécifique avec ces différentes cellules, mais d’autres molécules ou adhésines favorisent l’adhésion en se fixant sur leurs ligands spécifiques: LFA I (Iymphocyte fanction associated antigen) avec ICAM I (inter cellular adhesion molecule), CD2 avec LFA3, CD4 avec HLA II et CD8 avec HLA I.
Les molécules d’adhésion.
Les adhésines augmentent la liaison
du récepteur des cellules T à l’antigène :
3. Lymphocytes B
Les Iymphocytes B matures expriment à leur surface des immunoglobulines IgM ou IgD, qui jouent le rôle de récepteurs spécifiques de l’antigène, et différents marqueurs de surface, dont les molécules HLA de classe I et de classe II. Après stimulation antigénique, ils proliferent en présence d’IL-4, puis se différencient en plasmocytes en présence d’IL-6. Le plasmocyte sécrète initialement des immunoglobulines de type M, de même spécificité que l’IgM de surface exprimée par le Iymphocyte B, puis lors d’une seconde stimulation antigénique (réponse secondaire) des IgG ou d’autres immunoglobulines d’isotype différent (IgA ou E) exprimant la même région variable qui caractérise la reconnaissance de l’antigène.
4. Cellules NK (natural killer) et cellules K (killer)
Les cellules NK représentent environ 2 % des lymphocytes périphériques circulants. Non restreintes par le système majeur d’histocompatibilité, elles n’adhèrent pas et ne phagocytent pas, mais peuvent reconna~tre par leur récepteur pour le fragment Fc des immunoglobulines, différentes cellules cibles recouvertes d’anticorps. Leur cytotoxicité correspond alors au phénomène de cytotoxicité dépendante des anticorps (ADCC: antibody dependent cellular cytotoxicity), à médiation cellulaire en l’absence de complément. Ces cellules sont alors appelées cellules K.
Revenir au menu
Cytokines
Les cytokines, glycoprotéines solubles, sont sécrétées par certaines sous-populations Iymphocytaires T et par les monocytes. Elles agissent à distance lors d’une réaction inflammatoire mais surtout permettent l’activation des cellules du système immunitaire (lymphocytes B, T, macrophages), des cellules responsables des réponses cytotoxiques et de celles liées à l’hypersensibilité retardée.
L’interleukine 1(IL-1), sécrétée par les monocytesmacrophages, est la première cytokine intervenant dans la maturation et l’activation des Iymphocytes B et T après contact antigénique et contrôle l’induction des récepteurs de 1’IL-2.
L’interleukine 2 (IL-2) est au centre de la réaction de rejet de greffe et représente la cible de plusieurs traitements immunosuppresseurs (ciclosporine, anticorps monoclonaux). Elle est produite par les Iymphocytes T CD4+ Thl après stimulation antigénique en présence d’IL-1. L’IL-2 n’agit que sur les Iymphocytes T activés exprimant un récepteur de haute affinité pour cette cytokine (IL-2 R). Elle stimule leur prolifération, ainsi que la production de cytokines par les lymphocytes T CD4+ et la cytotoxicité des lymphocytes T CD8+. Elle est indispensable à l’expression de l’hypersensibilité retardée. Elle stimule également la prolifération des Iymphocytes B et la production d’immunoglobulines.
L’interleukine 4 (IL-4) synthétisée par les Iymphocytes T CD4+ Th2, agit sur la prolifération des Iymphocytes B, la production d’immunoglobulines et induit l’expression des antigènes de classe II. L’IL-4 peut également agir sur les macrophages en augmentant leur cytotoxicité.
L’interleukine 6 (IL-6) synthétisée par les monocytesmacrophages et les Iymphocytes B et T, induit la prolifération des Iymphocytes B et la différenciation en plasmocytes avec production d’immunoglobulines. Elle active les Iymphocytes T, induit la différenciation des Iymphocytes cytotoxiques et des monocytes en macrophages avec augmentation de la phagocytose.
L’interféron Gamma (IFN y), produit par les Iymphocytes T activés, est un puissant activateur des macrophages. Il augmente l’expression des molécules de classe II à la surface des macrophages et des Iymphocytes B. Il augmente également l’activité des Iymphocytes cytotoxiques et des cellules NK ainsi que sa propre synthèse.
Revenir au menu
Cellules productrices des cytokines
et principales actions
| Cytokines |
Cellules sécrétrices |
Actions principales |
| IL-1 |
Lymphocytes B et T Macrophages |
Prolifération des lymphocytes T activés par l’antigène |
| IL-2 |
Lymphocytes T CD4+ |
Prolifération des lymphocytes T4 Différenciation en lymphocytes cytotoxiques |
| IL-4 |
Lymphocytes T CD4+ |
Prolifération des lymphocytes B Augmentation de l’expression du HLA II à la surface des LB |
| IL-6 |
Monocytes Macrophages |
Différenciation en lymphocytes cytotoxiques, différenciation des lymphocytes B en plasmocytes |
| IFN gamma |
Lymphocytes T activés |
Augmentation de l’expression du HLA de classe II à la surface des macrophages et des lymphocytes B |
| TNF alpha |
Monocytes Macrophages Lymphocytes T |
Activation et chimiotactisme des polynucléaires neutrophiles |
Revenir au menu
Antigènes exprimés par les cellules du greffon
Trois groupes d’antigènes exprimés en abondance à la surface des membranes cellulaires sont impliqués dans les mécanismes immunologiques du rejet de greffe.
1. Antigènes du complexe majeur d’histocompatibilité (CMH ou HLA)
Les gènes codant les antigènes d’histocompatibilité, qui interviennent dans l’identité du soi (HLA classe I) et le contrôle du rejet du non soi ou régulation de la réponse immune (HLA classe II), sont situés sur le bras court du chromosome 6 et réunis dans le complexe majeur d’histocompatibilité (CMH) découvert par Jean Dausset en 1958. Le typage HLA d’un individu, initialement par technique sérologique ou de microlymphotoxicité et maintenant par biologie moléculaire, permet de définir les produits géniques issus de chaque chromosome parental et donc ses 2 haplotypes. Les antigènes HLA de classe I, sont la cible de la Iymphototoxicité due aux cellules T CD8+. Les antigènes HLA de classe II, qui présentent l’antigène aux cellules T CD4+, induisent la transformation blastique des cellules T dans la réaction Iymphocytaire mixte.
Les antigènes HLA de classe I sont constitués de 2 chaînes polypeptidiques: une chaîne lourde de 45 kDa, codée dans le CMH, qui porte la variabilité et est associée de facon non covalente à une chaîne légère, codée en dehors du CMH (chromosome 5), identique pour toutes les molécules: la ß2 microglobuline. Les antigènes HLA A et B sont les principaux antigènes HLA de classe I et correspondent aux produits des 2 locus majeurs de classe I du CMH: HLA A et HLA B. Il existe un troisième locus de classe I, HLA C, situé entre HLA A et B. Les antigènes HLA C sont moins immunogéniques et, en pratique, ont une importance moindre dans les typages tissulaires réalisés. Les antigènes HLA de classe I sont exprimés par toutes les cellules nucléées de l’organisme. Les cellules lymphoides expriment beaucoup plus d’antigènes HLA de classe I que les cellules parenchymateuses. À ce jour, plus de 120 allèles de HLA classe I ont été mis en évidence. De nouveaux gènes appartenant au système HLA classe I ont été récemment mis en évidence: E, F, G, H, J et pourraient avoir un rôle dans le rejet de greffe. Les antigènes HLA de classe II sont des glycoprotéines transmembranaires, hétérodimériques comportant une chaîne a et une chaîne ß associées de manière non covalente. La région du CMH codant les antigènes de classe II, appelée HLA D, est subdivisée en 3 sous-régions: HLA DP, DQ et DR. Les antigènes HLA de classe II sont exprimés par certains types cellulaires seulement: Iymphocytes B, macrophages, cellules endothéliales et cellules dendritiques. À ce jour, plus de 150 allèles ont été mis en évidence. L’expression des antigènes HLA, notamment de classe II, est augmentée pendant le rejet. Les infections virales associées à un rejet jouent le rôle d’inducteur puissant pour l’expression des antigènes HLA par l’intermédiaire d’une sécrétion d’IFN gamma.
2. Antigènes des groupes sanguins
Système ABO: les antigènes de groupes sanguins érythrocytaires ABO sont de puissants antigènes de transplantation. Le locus ABO a 3 allèles A, B et O : gènes A et B codominants, gène O récessif avec 4 génotypes possibles (A, B, AB, O). Les antigènes A et B sont présents sur les hématies, mais aussi sur certaines cellules épithéliales et endothéliales. Des anticorps anti-A ou anti-B immuns, encore appelés allo-anticorps, peuvent apparaître à la suite d’une immunisation (grossesse, transfusions). La compatibilité dans le système ABO doit être rigoureusement respectée pour toute transplantation d’organe.
Autres systèmes antigéniques des groupes sanguins: de nombreux autres alloantigènes sont portés par les globules rouges notamment antigène Rhésus, antigènes des groupes Kell, Duffy et Kidd. À la différence des antigènes A et B, il n’existe pas d’anticorps naturels contre ces autres systèmes antigéniques érythrocytaires, qui peuvent être néanmoins responsables d’allo-immunisation. En pratique, la compatibilité dans tous ces autres systèmes antigéniques des groupes sanguins n’est pas requise pour réaliser une transplantation d’organe.
3. Antigènes mineurs d’histocompatibilité
Le rôle de certains antigènes indépendants du CMH et du système ABO dans le rejet des greffes est démontré par la survenue de rejet chez des receveurs d’allogreffe HLA identiques. La nature des antigènes mineurs d’histocompatibilité est encore mal connue. Il s’agit principalement d’antigènes exprimés par les cellules endothéliales vasculaires et par les monocytes du donneur. Les cellules endothéliales qui expriment les antigènes de classe I et II, les antigènes du système ABO sont des cibles privilégiées des réactions de rejet. Le rôle des antigènes mineurs d’histocompatibilité est variable selon l’organe greffé. L’antigène érythrocytaire Lewis et des antigènes mâles, codés par le chromosome Y, pourraient être impliqués dans le rejet de greffe d’organe et dans la maladie du greffon contre l’hôte.
Revenir au menu
Mécanisme du rejet de greffe
L’étape initiale majeure de la réaction de rejet est la reconnaissance des antigènes étrangers du greffon par les éléments du système immunitaire après présentation par les cellules présentatrices d’antigènes aux lymphocytes T CD4+ qui permet alors l’activation en cascade et la différenciation des différentes cellules du système immunitaire. L’importance relative des différents mécanismes effecteurs du rejet est difficile à apprécier, mais tous concourent à l’apparition des lésions histologiques caractéristiques du rejet d’allogreffe.
Revenir au menu
Anticorps et complément : mécanisme humoral
Les anticorps présents chez le receveur se fixent sur un antigène du greffon. Le complexe antigène-anticorps active le système du complément, avec afflux et activation des polynucléaires neutrophiles et des macrophages, aboutissant à la Iyse cellulaire qui représente l’étape finale. Ce mécanisme explique le rejet vasculaire suraigu. Les anticorps préformés après sensibilisation préalable aux alloantigènes (notamment HLA de classe I et groupes sanguin A, B, O) sont détectés par la positivité du cross match avant la transplantation (sérum du receveur mis en présence avec les Iymphocytes B et T du donneur) qui contre-indique la greffe.
Revenir au menu
Cellules T cytotoxiques
Les cellules T CD8+, en collaboration avec les cellules T CD4+ qui sécrètent de l’IL-2, détruisent les cellules du greffon par reconnaissance des antigènes HLA de classe I (ou parfois de classe II), après contact, synthèse de perforine et Iyse de la membrane de la cellule-cible, ou bien par induction d’une apoptose (mort cellulaire programmée). Ce type de rejet, fréquent, avec infiltration du greffon par des cellules mononucléées, notamment des cellules T activées, peut entraîner une fibrose mutilante.
Revenir au menu
Cytotoxicité dépendante des anticorps: ADCC
Les cellules NK sont en nombre très important dans le greffon au cours des réactions de rejet. Les cellules K du receveur se fixent, par l’intermédiaire de leur récepteur du fragment Fc, sur les cellules du greffon recouvertes d’anticorps et entraînent leur Iyse sans intervention du complément. Ce mécanisme pourrait être mis en jeu dans les lésions de vascularite observées au cours du rejet chronique.
Revenir au menu
Hypersensibilité retardée
Les Iymphocytes CD4+ reconnaissant les antigènes HLA de classe II du greffon permettent de recruter et d’activer des macrophages. Ces derniers libèrent des enzymes Iysosomiales et entraînent la Iyse de la cellule cible du greffon. Peu de Iymphocytes T sont nécessaires pour recruter un grand nombre de macrophages et entraîner des dégâts cellulaires importants.
Revenir au menu
Expression clinique du rejet d’allogreffe d’organe
Le rejet est un phénomène constant, sans périodicité, dont le diagnostic est avant tout histologique. L’expression clinique du rejet de greffe varie selon des facteurs génétiques et la nature de l’organe transplanté.
 |

|
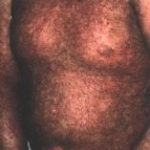
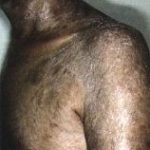
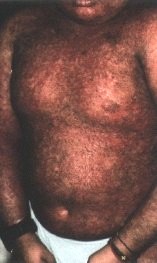
GVH cutanée chronique
(forme lichénienne) |
GVH cutanée chronique
(forme scléreuse) |
Revenir au menu
Rejet suraigu
Il se manifeste dans les heures qui suivent le rétablissement de la continuité vasculaire par un infarctus du transplant, parfois associé à une coagulopathie de consommation. Des rejets suraigus peuvent survenir en l’absence d’anticorps préformés détectés par le cross match.
Revenir au menu
Rejet aigu
Il survient à partir du 4e jour après la greffe et se traduit par des signes généraux, fonctionnels et biologiques qui varient selon l’organe transplanté.
1. Après transplantation rénale
Le rejet aigu précoce plus fréquent au cours des premiers mois peut associer: fièvre, augmentation du volume ou de la sensibilité du greffon, prise de poids avec chute de la diurèse, apparition ou majoration d’une hypertension artérielle. Biologiquement, apparaissent une insuffisance rénale, une baisse de la natriurèse et parfois une protéinurie. La biopsie rénale affirme le diagnostic et apprécie la gravité et l’étendue des lésions.
2. Après transplantation cardiaque
Le rejet aigu, plus fréquent dans les 6 premiers mois, est le plus souvent asymptomatique diagnostiqué par la surveillance échographique (diminution de la contractilité segmentaire ou globale) et histologique systématiques. Les signes cliniques ou électriques, beaucoup trop tardifs, témoignent d’un rejet aigu gravissime. La biopsie endomyocardique permet d’affirmer le diagnostic et de classer le rejet selon sa gravité histologique.
3. Après transplantation pulmonaire
Le rejet reste souvent asymptomatique et est diagnostiqué par la surveillance systématique clinique, spirométrique (baisse du peak-flow et les débits distaux) et radiologique (infiltrats interstitiels parfois seulement visibles au scanner). Les biopsies transbronchiques avec lavage bronchio-alvéolaire permettent de différencier l’infection du rejet, qui peuvent coexister, et d’apprécier la sévérité histologique des lésions.
4. Après transplantation hépatique
Le rejet aigu peut être asymptomatique ou se traduire cliniquement par une asthénie, une fièvre, une hépatomégalie, une ascite ou un ictère. Souvent, seules des anomalies biologiques isolées, cholestase ou cytolyse, motivent la biopsie qui va confirmer la diagnostic.
5. Après transplantation pancréatique
La survenue du rejet pose un problème diagnostique en l’absence de marqueur précoce du rejet du pancréas endocrine. En cas de greffe combinée rein-pancréas, l’élévation de la créatininémie est considérée comme le marqueur le plus fiable du rejet pancréatique. La biopsie à l’aiguille, délicate techniquement et non dénuée de risques, reste d’interprétation difficile.
Revenir au menu
Rejet chronique
Le rejet chronique, d’étiologie multiple mais avant tout immunologique, est responsable d’une altération progressive et irréversible de la fonction du greffon. Histologiquement, il réalise une vasculopathie chronique spécifique de l’organe greffé, essentiellement fibrosante et proliférante. Les lésions d’artériosclérose accélérée du greffon diffèrent de celles de l’athérome classique, car elles sont diffuses et circonférentielles, avec hyperplasie concentrique de l’intima, respectant la limitante élastique interne et d’évolution rapide en quelques mois.
La symptomatologie du rejet chronique varie selon l’organe greffé. Après transplantation rénale, il se traduit par une insuffisance rénale lentement progressive et une hypertension artérielle parfois associées à une protéinurie. Après transplantation cardiaque, se développe une coronaropathie chronique indolore, car l’angor est asymptomatique sur un coeur dénervé. L’apparition de signes cliniques d’insuffisance cardiaque est très tardive. Après transplantation pulmonaire, apparaissent des lésions de bronchiolite oblitérante avec symptômes d’insuffisance respiratoire chronique (dyspnée, surinfection). Après transplantation hépatique, le rejet chronique se traduit par une cholestase biologique isolée, puis par un ictère progressif évoluant vers une insuffisance hépatocellulaire. Après transplantation pancréatique, réapparaissent une insulinodépendance et (ou) une insuffisance rénale en cas de transplantation rein-pancréas.
Dans tous les cas, le seul traitement du rejet chronique est la retransplantation avec un risque de récidive accrue sur le deuxième greffon. Le meilleur traitement est avant tout préventif par le diagnostic et le traitement précoces des épisodes de rejet aigus et la lutte contre les autres facteurs de risque de la maladie athéromateuse (voir: « pour approfondir » à la fin de ce document).
Revenir au menu
Mécanismes et expression clinique de la maladie du greffon contre l’hôte
Lorsque le receveur est incapable de rejeter une greffe allogénique, par déficit immunitaire pathologique ou consécutif à l’immunosuppression, et si le greffon contient des lymphocytes T, ces derniers peuvent reconnaître les antigènes du receveur et induire une réaction du greffon contre l’hôte (GVHD: graft versus host disease). La GVHD nécessite :
1) une différence d’histocompatibilité entre donneur et receveur;
2) la présence de cellules immunocompétentes dans le greffon capables de réagir contre les antigènes d’histocompatibilité de l’hôte
3) une impossibilité du receveur de rejeter la greffe.
Les mécanismes immunologiques sont incomplètement connus, mais la GVHD est liée à l’activation des lymphocytes T matures du greffon (donneur) qui reconnaissent les antigènes majeurs et mineurs différents du système HLA du receveur. L’activité cytotoxique est, soit directe par les Iymphocytes CD8+, soit indirecte par le recrutement d’autres cellules effectrices et la sécrétion de cytokines (IFN gamma, IL-1, TNF). Certains agents microbiens, notamment à partir de la flore digestive, pourraient avoir une antigénicité croisée avec des alloantigènes de l’hôte ou causer une activation non spécifique des macrophages ou des cellules présentatrices d’antigènes.
Revenir au menu
GVHD aiguë
Elle survient généralement dans les 100 jours suivant la greffe, la plupart du temps entre 2 et 5 semaines, avec une fréquence de 30 à 70 % selon la greffe considérée malgré le traitement préventif. Les trois organes cibles sont: la peau, le foie et le tube digestif. La GVHD aiguë est classée en 4 grades de gravité croissante, selon le degré d’atteinte des 3 organes-cibles et avec altération plus ou moins marquée de l’état général: grades I et II de pronostic favorable, grade III de pronostic réservé, grade IV presque toujours mortel.
Score clinique de sévérité de l’atteinte des
organes-cibles au cours de la GVHD aiguë
Peau
| Sévérité |
Peau |
| + |
Eruption < 25% Surface Corporelle |
| ++ |
Eruption 25-50% Surface Corporelle |
| +++ |
Eruption généralisée |
| ++++ |
Epidermolyse bulleuse |
Foie
| Sévérité |
Foie |
| + |
Bilirubine : 10-30 mg/l |
| ++ |
Bilirubine : 30-60 mg/l |
| +++ |
Bilirubine : 60-150 mg/l |
| ++++ |
Bilirubine : > 150 mg/l |
Tube digestif
| Sévérité |
Tube Digestif |
| + |
Diarrhée > 500 ml/24h |
| ++ |
Diarrhée > 1000 ml/24h |
| +++ |
Diarrhée > 1500 ml/24h |
| ++++ |
Douleurs abdominales sévères ou hémorragies |
Grades de sévérité de la GVHD aiguë
| Grade |
Peau |
Foie |
Tube Digestif |
Altération de l’état général |
| I |
+ à ++ |
0 |
0 |
0 |
| II |
+ à +++ |
+ |
+ |
Discrète |
| III |
++ à +++ |
> ++ |
> ++ |
Marquée |
| IV |
>=++ |
>=++ |
>=++ |
Sévère |
1. Peau
Il s’agit d’une éruption maculopapuleuse, prurigineuse, inflammatoire, d’évolution fluctuante, touchant le visage, la paume des mains et la plante des pieds, douloureuse dans les deux derniers territoires. Elle peut s’étendre au tronc, à la racine des membres puis à l’ensemble du tégument. Toutes les formes sont possibles depuis l’éruption localisée jusqu’au syndrome de Lyell. Les muqueuses peuvent être atteintes (conjonctive, organes génitaux externes). Le diagnostic de certitude est histologique: foyers de nécrose, vacuolisation des cellules basales de l’épiderme, oedème et infiltration du sous-épiderme et habituellement mais inconstamment en immunomarquage, des Iymphocytes T CD8+.
2. Tube digestif
L’atteinte du tube digestif est souvent retardée. Elle s’exprime typiquement par une diarrhée à quantifier, avec douleurs abdominales et vomissements. Des hémorragies digestives sont possibles. En cas d’atteinte colique basse, un syndrome rectal peut être au premier plan. Les biopsies, rarement indiquées, peuvent révéler une atrophie villositaire, une destruction des cryptes intestinales et une infiltration Iymphocytaire de la lamina propria.
3. Foie
L’atteinte hépatique se traduit par un ictère d’intensité variable, avec cytolyse initiale régressant progressivement alors que se développe une cholestase sans insuffisance hépatocellulaire. L’histologie retrouve des foyers de nécrose éosinophile, une destruction des canaux biliaires, une hypertrophie des cellules de Küpffer et des infiltrats lymphocytaires péribiliaires. Elle est indispensable au pronostic et guide le traitement.
Revenir au menu
GVHD chronique
Par définition, la GHVD chronique, généralement mais non constamment précédée par une GVHD aiguë, apparaît plus de 100 jours après la greffe, mais ses manifestations peuvent être plus précoces. Elle survient chez environ 50 % des patients et atteint, à des degrés variables, la peau, les muqueuses et le foie. Elle est classée en formes limitées [peau et (ou) maladies hépatiques] ou extensives. La symptomatologie de la GVHD chronique évoque certaines maladies systémiques, dites « auto-immunes » (sclérodermie, syndrome de Gougerot-Sjögren ou cirrhose biliaire primitive). La GVHD chronique entraîne la persistance d’un déficit immunitaire responsable d’infections tardives potentiellement mortelles (infections à CMV, aspergillose).
1. Peau et muqueuses
L’atteinte cutanée est quasi constante avec des zones d’hyper ou d’hypopigmentation, planes (type lichen plan) ou associées à des papules, avec des formes lichéniennes ou scléreuses. Il peut s’agir d’une éruption érythémateuse diffuse avec desquamation survenant après exposition solaire, sur un territoire irradié ou sur des lésions infectieuses (zona). L’atteinte muqueuse entraîne un syndrome sec buccal et oculaire de type syndrome de Gougerot-Sjögren. Histologiquement, existent une nécrose épithéliale, un infiltrat mononucléé riche en cellules CD8+ et une fibrose épithéliale et sous-épithéliale.
2. Foie
L’atteinte hépatique, très fréquente (95 % des cas), se traduit par une cytolyse hépatique d’intensité variable et une cholestase parfois responsable d’un ictère. Elle peut mimer une cirrhose biliaire primitive. Le diagnostic est surtout histologique: atteinte des canaux biliaires majeure avec parfois leur destruction complète, infiltrats inflammatoires péribiliaires avec différenciation plasmocytaire et destruction hépatocytaire au contact des lymphocytes.
3. Autres manifestations
La GVHD chronique s’accompagne de l’apparition d’autoanticorps dans 10 à 60 % des cas: anticorps antinucléaires, anticorps anti-DNA et anti-muscle lisse, plus récemment anticorps anticytosquelette et antinucléolaires. Des tableaux évolués peuvent être observés avec différentes atteintes évocatrices d’une maladie systématique proche de la sclérodermie. L’atteinte oculaire, parfois asymptomatique dépistée par le test de Shirmer, est caractérisée par une kérato-conjonctivite sèche avec irritation et photophobie. L’atteinte pulmonaire grave réalise un tableau de bronchiolite oblitérante avec pneumopathie obstructive résistante aux bronchodilatateurs, qui assombrit le pronostic vital. L’atteinte digestive est rare au cours de la GVHD chronique, mais peut entrâîner des troubles de la motricité oesophagienne. Des neuropathies périphériques, polymyosites voire myasthénies sont possibles. Les arthropathies sont secondaires aux rétractions tendineuses et à l’amyotrophie d’origine mixte, spécifique lice à la GVHD, et cortisonique.
Points Forts à Retenir
Les manifestations cliniques du rejet d’allogreffe sont tardives après transplantations d’organes et le diagnostic de rejet aigu repose avant tout sur l’histologie du greffon.
Dans la forme aiguë de la GVHD, les organes cibles sont : la peau, le foie et le tube digestif.
Dans la forme chronique de la GVHD, les organes-cibles principaux sont la peau et le foie. Les manifestations cliniques et biologiques peuvent prendre l’aspect de maladies systémiques telles qu’un syndrome de Gougerot-Sjögren, une sclérodermie ou une cirrhose biliaire primitive.
Pour approfondir…
« Principe de traitement du rejet aigu du greffon après transplantation d’organe »
Il dépend de la sévérité et de la nature de l’organe transplanté et repose classiquement sur une corticothérapie à forte dose en bolus intraveineux pendant 3 jours. L’efficacité du traitement est jugée rapidement sur la régression des signes cliniques ou biologiques, échograpaiques ou radiologiques et (ou) sur les résultats d’une biopsie de contrôle. En cas d’échec, un traitement immunosuppresseur plus important par répétition des bolus de corticoïdes intraveineux seuls ou associés à une cure de 3 à 10 jours de sérum anti-lymphocytaire poly ou monoclonal, parfois suivi d’une augmentation de la corticothérapie per os à la dose de 1 mg/kg par jour avec décroissance secondaire, permet en règle générale de contrôler le rejet. Les rejets suraigus irréversibles sont extrêmement rares et surviennent soit très précocement soit en cas de retard diagnostique. La prévention du rejet aigu repose sur le maintien du traitement immunosuppresseur de fond et l’acquisition progressive d’une tolérance du greffon.